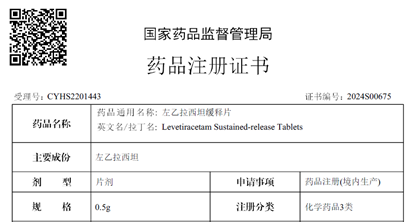
近日���,越洋醫藥自主研發(fā)的左乙拉西坦緩釋片(500mg)獲得國家藥品監督管理局(NMPA)上市批準�����,批準文號:國藥準字H20243583����,該產(chǎn)品為《國家基本醫療保險��、工傷保險和生育保險藥品目錄》醫保乙類(lèi)產(chǎn)品�。左乙拉西坦作為多國指南推薦的抗癲癇優(yōu)選藥物����,可用于癲癇的單獨治療��,其緩釋制劑為每日一次服藥����,避免了因普通制劑血藥濃度波動(dòng)而引起的癲癇發(fā)作風(fēng)險�。此規格的獲批標志著(zhù)中美雙報雙獲批圓滿(mǎn)收官��。2022年左乙拉西坦全球銷(xiāo)售額超25億美元���,中國銷(xiāo)售額近10億元��,中國院內銷(xiāo)售額增長(cháng)達13%左右�����。目前此產(chǎn)品正在尋找中國和其他國家的商業(yè)化合作伙伴�。
公司召開(kāi)了產(chǎn)品獲批慶功會(huì )����,會(huì )上項目組成員紛紛發(fā)表了獲獎感言���,表達對公司的祝賀和感激��。公司首席技術(shù)官范軍博士發(fā)言講述了產(chǎn)品從研發(fā)��、生產(chǎn)�����、臨床到注冊申報��、FDA現場(chǎng)核查及缺陷信答復的種種挑戰�,獲批是起點(diǎn)也是公司轉型商業(yè)化的開(kāi)始��,這是大家齊心協(xié)力����、團結一致的結果�。最后�,越洋創(chuàng )始人���、董事長(cháng)兼CEO聞曉光博士表達了對全體越洋人的感謝��,強調雖然實(shí)現了中美雙報雙獲批“零”的突破���,但這只是萬(wàn)里長(cháng)征邁出的第一步�����,強調越洋人要繼續秉承只為成功找出路不為失敗找借口的工作理念����,不忘初心�,真正把緩控釋新藥在中美等多國獲批上市�����,做到越洋銷(xiāo)售全球��,給患者帶來(lái)療效更優(yōu)����、副作用更小��、順應性更好的新藥�����,這樣公司才能做得更好�、走得更遠�。



2011年12月成立��,廣州�,江蘇泰州和美國加州圣地亞哥擁有研發(fā)及中試放大基地�����,擁有多名全職歐美海歸及本土骨干人才����,擁有100+名員工及10000多平方米基地����。20+新藥獲批中美臨床批件���,10+新藥處于I期和III期臨床階段����,一個(gè)緩控釋產(chǎn)品在中國和美國獲批上市許可����。
主營(yíng)業(yè)務(wù)
—上市許可持有人
應用越洋專(zhuān)有和通用緩控釋技術(shù)開(kāi)發(fā)針對美國市場(chǎng)的NDA(505(b)(2))申報路徑)和中國市場(chǎng)的2類(lèi)新藥��;委托生產(chǎn)���,委托銷(xiāo)售�。
—產(chǎn)品開(kāi)發(fā)技術(shù)服務(wù)
借助公司的專(zhuān)有平臺技術(shù)(UC-trol?, Mech-trol?, Bi-lock?)以及通用平臺技術(shù)(Multi-layer, Tablet-in-tablet, Osmotic Pump)服務(wù)客戶(hù)����,1)提高NCE的成藥性�����;2)把客戶(hù)的一代普通制劑進(jìn)行迭代創(chuàng )新轉化成緩控釋新藥�,延長(cháng)產(chǎn)品壽命�,3)為國內外客戶(hù)開(kāi)發(fā)緩控釋仿制藥���。
—產(chǎn)品共同開(kāi)發(fā)
希望與值得信賴(lài)的合作伙伴共同開(kāi)發(fā)已進(jìn)入不同臨床研究階段的緩控釋新藥產(chǎn)品�;聯(lián)合開(kāi)發(fā)在中美已獲得臨床試驗許可的緩控釋新藥產(chǎn)品�。公司產(chǎn)品涉及疼痛��、失眠���、癲癇�����、抑郁癥���、高血壓��、糖尿病�����、類(lèi)風(fēng)濕性關(guān)節炎等多個(gè)適應證領(lǐng)域���。
—產(chǎn)品權益轉讓
國內外獲批的臨床批件����,不同臨床階段的產(chǎn)品及生產(chǎn)批件轉讓給國內外藥企�,越洋醫藥獲得轉讓費和銷(xiāo)售提成��。